INFORMACIÓ TEÒRICA - EL CICLE CEL·LULAR
La vida d’una cèl·lula té diferents etapes i va des que neix fins que es divideix, o fins que mor.
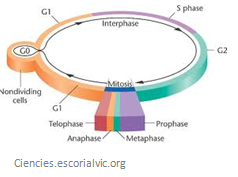
Per tant se separa el cicle cel·lular en dues grans etapes, la interfase i la divisió (també anomenada fase M).
Interfase
La interfase és el període comprès entre dues divisions i el més llarg, té tres fases:
- Fase G1: és la fase de creixement d’una cèl·lula que prové d’una divisió. En aquesta etapa hi ha una despesa important d’energia perquè els gens es transcriuen i es tradueixen per poder obtenir les proteïnes que calen per a que la cèl·lula creixi, ja que duplicarà la seva mida i la seva massa.
- Fase S (síntesi): quan la cèl·lula ja ha crescut prou durant la fase G1 duplica el seu material genètic. Aquest procés és una preparació per a la divisió, perquè així la cèl·lula hi arribarà amb dues còpies idèntiques del genoma i es dividirà donant lloc a dues cèl·lules filles amb la mateixa quantitat de material genètic que la cèl·lula tenia en fase G1. Com a resultat de la rèplica del DNA cada cromosoma, que estava format per una cromàtide, es duplica i queda format per dues cromàtides iguals.
- Fase G2: és la fase que hi ha just abans de la divisió, la cèl·lula ha de transcriure i traduir els gens de les proteïnes necessàries per a la divisió cel·lular. Aquesta fase acaba quan la cromatina (forma en la que es troba el material genètic durant la interfase) comença a condensar-se.
En alguns casos també es pot trobar la fase G0, on hi entraria la cèl·lula després de la divisió. En aquesta fase la cèl·lula experimentaria una sèrie de transformacions, això és perquè hi ha diferenciació cel·lular, la cèl·lula s’especialitza.
Divisió
Després d’aquestes fases ve la de divisió, en aquest cas explicaré la divisió cel·lular que porta a terme una cèl·lula animal somàtica (cèl·lules comunes del cos i no les cèl·lules germinals).
Durant la divisió una cèl·lula progenitora es divideix i dóna lloc a dues cèl·lules filles idèntiques, ja que es reparteixen equitativament el contingut nuclear, o sigui el material genètic durant la mitosi, i el material citoplasmàtic, com ara els orgànuls, durant al citocinesi.
Fases de la mitosi:
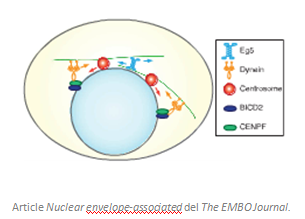
- Profase: la cromatina (estat del material genètic durant la interfase) es condensa formant cromosoma. Un cromosoma conté dues cromàtides germanes, resultants del procés de síntesi en la fase s, unides pel centròmer. En els dos centrosomes que hi ha a prop del nucli comencen a créixer microtúbuls que formen l’àster, polimeritzats a partir de la tubulina soluble del citoplasma. Algunes proteïnes motores, com la cinesina Eg5, s’encarreguen de crear forces repulsives per poder empènyer els centrosomes a extrems oposats del nucli. Ja que els dos àsters estan en contacte però a mesura que progressa la profase es van separant i es col·locaran en pols oposats fins a formar el fus. El fus mitòtic està format per microtúbuls polars, que provenen dels àsters, i per microtúbuls del cinetocor, que provenen del cinetocor de cada cromàtida.
També el nuclèol va disminuint fins que desapareix.
Per tant se separa el cicle cel·lular en dues grans etapes, la interfase i la divisió (també anomenada fase M).
Interfase
La interfase és el període comprès entre dues divisions i el més llarg, té tres fases:
- Fase G1: és la fase de creixement d’una cèl·lula que prové d’una divisió. En aquesta etapa hi ha una despesa important d’energia perquè els gens es transcriuen i es tradueixen per poder obtenir les proteïnes que calen per a que la cèl·lula creixi, ja que duplicarà la seva mida i la seva massa.
- Fase S (síntesi): quan la cèl·lula ja ha crescut prou durant la fase G1 duplica el seu material genètic. Aquest procés és una preparació per a la divisió, perquè així la cèl·lula hi arribarà amb dues còpies idèntiques del genoma i es dividirà donant lloc a dues cèl·lules filles amb la mateixa quantitat de material genètic que la cèl·lula tenia en fase G1. Com a resultat de la rèplica del DNA cada cromosoma, que estava format per una cromàtide, es duplica i queda format per dues cromàtides iguals.
- Fase G2: és la fase que hi ha just abans de la divisió, la cèl·lula ha de transcriure i traduir els gens de les proteïnes necessàries per a la divisió cel·lular. Aquesta fase acaba quan la cromatina (forma en la que es troba el material genètic durant la interfase) comença a condensar-se.
En alguns casos també es pot trobar la fase G0, on hi entraria la cèl·lula després de la divisió. En aquesta fase la cèl·lula experimentaria una sèrie de transformacions, això és perquè hi ha diferenciació cel·lular, la cèl·lula s’especialitza.
Divisió
Després d’aquestes fases ve la de divisió, en aquest cas explicaré la divisió cel·lular que porta a terme una cèl·lula animal somàtica (cèl·lules comunes del cos i no les cèl·lules germinals).
Durant la divisió una cèl·lula progenitora es divideix i dóna lloc a dues cèl·lules filles idèntiques, ja que es reparteixen equitativament el contingut nuclear, o sigui el material genètic durant la mitosi, i el material citoplasmàtic, com ara els orgànuls, durant al citocinesi.
Fases de la mitosi:
- Profase: la cromatina (estat del material genètic durant la interfase) es condensa formant cromosoma. Un cromosoma conté dues cromàtides germanes, resultants del procés de síntesi en la fase s, unides pel centròmer. En els dos centrosomes que hi ha a prop del nucli comencen a créixer microtúbuls que formen l’àster, polimeritzats a partir de la tubulina soluble del citoplasma. Algunes proteïnes motores, com la cinesina Eg5, s’encarreguen de crear forces repulsives per poder empènyer els centrosomes a extrems oposats del nucli. Ja que els dos àsters estan en contacte però a mesura que progressa la profase es van separant i es col·locaran en pols oposats fins a formar el fus. El fus mitòtic està format per microtúbuls polars, que provenen dels àsters, i per microtúbuls del cinetocor, que provenen del cinetocor de cada cromàtida.
També el nuclèol va disminuint fins que desapareix.
-
Prometafase: la membrana nuclear es degrada, així hi haurà
prou espai per construir el fus mitòtic i portar a terme la divisió. Cada
cromosoma forma dos cinetocors al seu centròmer, un per cada cromàtida germana.
El cinetocor està format per proteïnes i farà de “ganxo” pels microtúbuls, serà
el punt per on s’enganxin els microtúbuls al cromosoma. Els cromosomes es
comencen a situar sobre els filaments del fus mitòtic gràcies als cinetocors.
Els microtúbuls del cinetocor interaccionen amb els microtúbuls polars i amb
aquesta interacció cada cromosoma s’orienta respecte l’eix del fus i es
desplaça fins al pla metafàsic.
- Metafase: després de les interaccions dels cromosomes, el conjunt d’aquests queda disposat a l’equador de la cèl·lula, a mig camí entre els dos pols cel·lulars, sobre el fus mitòtic.
- Anafase: comença quan els dos cinetocors d’un mateix cromosoma se separen, així cada cromàtide germana és arrossegada cap al pol oposat de la cèl·lula. Els microtúbuls del cinetocor es van escurçant, així els cromosomes s’acosten als pols, que es van separant cada vegada més.
- Telofase: quan les cromàtides arriben als pols corresponents de la cèl·lula els microtúbuls dels cinetocors desapareixen i es forma una nova membrana nuclear entorn de les cromàtides. La cromatina es torna a expandir i els nuclèols a aparèixer.
Després de la divisió del material genètic, la cèl·lula porta a terme la citocinesi per dividir el citoplasma. Aquest procés, en cèl·lules animals, es basa una segmentació que sol començar al final de la telofase i consisteix en estrangular la membrana citoplasmàtica a la zona central de la cèl·lula perpendicular a l’eix del fus mitòtic.
Regulació del cicle cel·lular
Per a que totes aquestes etapes es portin a terme correctament hi ha tot un gran mecanisme de regulació al darrere dels components que interactuen en les fases que hem vist. Aquests mecanismes s’encarreguen de controlar la duració i el canvi d’etapa, i també que no se’n repeteixi cap.
- Cinases dependent de ciclina
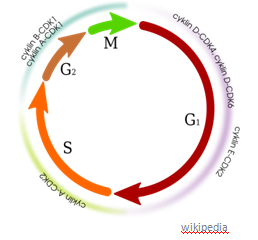
En la regulació del cicle cel·lular prenen molta importància les cinases dependents de ciclina (CDK), que són enzims constituïts per ciclina i per cinasa. El pas d’una fase del cicle a una altra ha de tenir lloc d’una manera organitzada, per tant, regulada per una sèrie de proteïnes cel·lulars entre les quals es troben les CDKs, que són una família de proteïnes que són activades en punts específics del cicle cel·lular. Tot i que s’han identificat fins a 11 tipus de CDK, les que tenen un paper més important durant el cicle cel·lular en són 4 (CDK4, CDK6, CDK2 i CDK1), i per a cada fase hi ha una o unes CDKs més rellevants.
L’activació de les CDKs es necessària perquè així puguin desencadenar diversos processos cel·lulars a partir de la fosforilació dels seus substrats. La CDK7 en combinació amb la ciclina H és la que té la funció de fosforilar i activar les altres CDKs.
Per tant una regulació dels nivells de CDKs és important per aconseguir una bona progressió del cicle cel·lular.
Aquí també agafen importància les ciclines ja que són les activadores d’aquestes cinases, sense les quals no podrien regular el cicle. Els nivells de CDKs són estables al llarg del cicle, però els de les ciclines varien, per tant no sempre les CDKs estan activades. Si les CDKs no estan activades, o sigui en absència de ciclina, el centre actiu de l’enzim CDK es troba parcialment tapat per una regió de la mateixa proteïna que no s’apartarà del centre actiu fins que no s’uneixi la ciclina a la CDK.
És per això que existeixen tractaments contra el càncer que ataquen aquestes CDKs, les inhibeixen per fer aturar el cicle cel·lular en una fase determinada. Ja que, per exemple, per a l’entrada a la mitosi cal el complex determinat ciclina B-CDK1.
Per passar d’una fase a una altra, a part de l’activació del complex corresponent també cal l’eliminació del complex anterior, cosa que es porta a terme al proteasoma. El proteasoma és un orgànul que degrada aquelles proteïnes que contenen una seqüència determinada d’ubiquitina.
- Metafase: després de les interaccions dels cromosomes, el conjunt d’aquests queda disposat a l’equador de la cèl·lula, a mig camí entre els dos pols cel·lulars, sobre el fus mitòtic.
- Anafase: comença quan els dos cinetocors d’un mateix cromosoma se separen, així cada cromàtide germana és arrossegada cap al pol oposat de la cèl·lula. Els microtúbuls del cinetocor es van escurçant, així els cromosomes s’acosten als pols, que es van separant cada vegada més.
- Telofase: quan les cromàtides arriben als pols corresponents de la cèl·lula els microtúbuls dels cinetocors desapareixen i es forma una nova membrana nuclear entorn de les cromàtides. La cromatina es torna a expandir i els nuclèols a aparèixer.
Després de la divisió del material genètic, la cèl·lula porta a terme la citocinesi per dividir el citoplasma. Aquest procés, en cèl·lules animals, es basa una segmentació que sol començar al final de la telofase i consisteix en estrangular la membrana citoplasmàtica a la zona central de la cèl·lula perpendicular a l’eix del fus mitòtic.
Regulació del cicle cel·lular
Per a que totes aquestes etapes es portin a terme correctament hi ha tot un gran mecanisme de regulació al darrere dels components que interactuen en les fases que hem vist. Aquests mecanismes s’encarreguen de controlar la duració i el canvi d’etapa, i també que no se’n repeteixi cap.
- Cinases dependent de ciclina
En la regulació del cicle cel·lular prenen molta importància les cinases dependents de ciclina (CDK), que són enzims constituïts per ciclina i per cinasa. El pas d’una fase del cicle a una altra ha de tenir lloc d’una manera organitzada, per tant, regulada per una sèrie de proteïnes cel·lulars entre les quals es troben les CDKs, que són una família de proteïnes que són activades en punts específics del cicle cel·lular. Tot i que s’han identificat fins a 11 tipus de CDK, les que tenen un paper més important durant el cicle cel·lular en són 4 (CDK4, CDK6, CDK2 i CDK1), i per a cada fase hi ha una o unes CDKs més rellevants.
L’activació de les CDKs es necessària perquè així puguin desencadenar diversos processos cel·lulars a partir de la fosforilació dels seus substrats. La CDK7 en combinació amb la ciclina H és la que té la funció de fosforilar i activar les altres CDKs.
Per tant una regulació dels nivells de CDKs és important per aconseguir una bona progressió del cicle cel·lular.
Aquí també agafen importància les ciclines ja que són les activadores d’aquestes cinases, sense les quals no podrien regular el cicle. Els nivells de CDKs són estables al llarg del cicle, però els de les ciclines varien, per tant no sempre les CDKs estan activades. Si les CDKs no estan activades, o sigui en absència de ciclina, el centre actiu de l’enzim CDK es troba parcialment tapat per una regió de la mateixa proteïna que no s’apartarà del centre actiu fins que no s’uneixi la ciclina a la CDK.
És per això que existeixen tractaments contra el càncer que ataquen aquestes CDKs, les inhibeixen per fer aturar el cicle cel·lular en una fase determinada. Ja que, per exemple, per a l’entrada a la mitosi cal el complex determinat ciclina B-CDK1.
Per passar d’una fase a una altra, a part de l’activació del complex corresponent també cal l’eliminació del complex anterior, cosa que es porta a terme al proteasoma. El proteasoma és un orgànul que degrada aquelles proteïnes que contenen una seqüència determinada d’ubiquitina.
- Punts de control
També són importants els punts de control que tenen lloc per controlar i assegurar que tot va seguint de la forma en que s’espera i que es pot continuar.
Aquestes vies de control són transitòries, o sigui desapareixen una vegada està resolt el problema que les ha posat en marxa i caduquen si el problema no s’ha resolt al cap d’un temps.
Lodish i els seus alumnes al 2005 van descriure els diferents punts de control que té el cicle cel·lular, per exemple n’hi ha un que s’anomena punt de control del dany del DNA, que pot funcionar en G1, S o G2, i ho fa de la següent manera: el dany genètic activarà la proteïna p53, que afavoreix la reparació del DNA i detindrà el cicle. En el cas que tot falli o que el dany sigui massa gran, estimularà l’apoptosi, la mort cel·lular programada.
- Cicle cel·lular i càncer
El càncer és una malaltia en que un grup de cèl·lules desenvolupen un creixement descontrolat, tenen una proliferació massa ràpida, es divideixen més enllà dels límits normals. Aquest grup de cèl·lules s’anomenen tumor i pot arribar a envair i destruir els teixits adjacents, i fins i tot pot escampar-se per diferents llocs del cos per via sanguínia o limfàtica i produir metàstasi.
Càncer i cicle cel·lular van molt lligats, perquè sabem que les cèl·lules cancerígenes es divideixen sense control, tenen un cicle cel·lular accelerat. Per tant una bona manera d’aturar el creixement d’un tumor, la proliferació de cèl·lules cancerígenes és deixar estancada la cèl·lula cancerígena en un dels estadis del cicle cel·lular, condemnant-la així a la impossibilitat de créixer més, de dividir-se i finalment a l’apoptosi.
La majoria de fàrmacs contra el càncer són fàrmacs que actuen contra la proliferació. Aquests fàrmacs el que fan és destorbar el cicle cel·lular, en diferents fases d’aquest. Per exemple n’hi ha que danyen el DNA o d’altres que funcionen com a inhibidors de cinasa dependent de ciclina.
Per tant hi ha diferents estratègies. En el meu treball he fixat la mitosi com si fos el “taló d’ Aquiles del càncer”, ja que sinó es pot realitzar la mitosi no es continua amb el cicle cel·lular i encara menys amb la proliferació cel·lular.
Medema i Jansen publicaren al 2011 un article explicant diversos procediments i investigacions portades a terme per poder frenar la proliferació de cèl·lules cancerígenes fixant la mitosis com a objectiu.
Una manera d’aturar la mitosi és allargar el punt de control de mitosi o de formació del fus acromàtic, ja que incrementar la durada de la mitosi acaba fent morir les cèl·lules mitòtiques. Hi ha substàncies com les taxanes i vinca alkaloids, una classe de drogues antimitòtiques que afecten la dinàmica dels microtúbuls. Causen formes anormals del fus acromàtic i això fa que els cromosomes no es puguin alinear correctament.
Quan això passa el punt de control s’atura, deixant un temps a la cèl·lula per corregir els errors, per tant s’està esperant massa estona per passar a l’anafase. Aquest temps d’espera ve donat per la senyal d’un grup de proteïnes.
Les substàncies que provoquen un alineament erroni dels cromosomes faran que la cèl·lula s’aturi en el punt de control de la mitosis, l’arrest mitòtic serà tan llarg que portarà la cèl·lula a la mort cel·lular. A part de portar a la mort cel·lular també s’ha vist en casos que es produeix una sortida de la mitosi (mitotic slippage), o sigui que la cèl·lula, tot i els seus errors, retrocedirà de fase mitòtica i tornarà a entrar en el cicle cel·lular. Però causarà una aneuploïdia perquè tornarà a començar el cicle cel·lular amb el doble de material genètic.
Les drogues convencionals microtubulars anomenades recentment (taxanes i vinca alkaloids) són efectives en alguns tractaments de càncer. Però hi ha una família de fàrmacs bastant nova, les Epothilones que són més suaus que les taxanes i tenen una estructura química que li fa tenir més afinitat pels microtúbuls. S’estan provant en assaigs clínics.
Però les substàncies que alteren la naturalesa dels microtúbuls tenen efectes secundaris. Aquests efectes es deuen a que aquestes substàncies impossibiliten la realització total i normal d’una mitosi (ja que els microtúbuls participen activament, formant el fus acromàtic), per tant frena la proliferació cel·lular a nivell general, no només el de cèl·lules cancerígenes. Aquesta frenada de la proliferació pot portar a una mielosupressió, una disminució de la medul·la òssia, disminuint així la producció d’eritròcits i de plaquetes. També és molt possible l’adquisició de certa resistència a aquests fàrmacs en diferents pacients segons com s’ha observat.
Per tant encara que veiem que l’acció de retardar la mitosi (efectiu amb aquests fàrmacs microtubulars) sembla tenir un efecte relativament citotòxic sobre el teixit cancerós, els efectes secundaris lligats a aquestes substàncies antimitòtiques en restringeixen l’aplicació.
Això va fer començar una recerca per trobar fàrmacs més selectius en quant a cèl·lules mitòtiques a les quals dirigir-se. Cal trobar punts febles de la mitosi per dissenyar fàrmacs específics.
Un dels objectius per aquest enfocament de tractament selectiu és fixar-se en la proteïna cinesina-5 (Eg5), una proteïna motora que pot unir-se a la superfície d’un microtúbul i desplaçar-s’hi longitudinalment arrossegant una càrrega mitjançant ATP com a font d’energia. La funció principal de la Eg5 és el transport de components cel·lulars. Doncs bé, aquesta proteïna durant la mitosi té la capacitat de portar a terme la separació dels centrosomes durant la profase, això iniciaria la construcció d’un fus acromàtic bipolar. Si inhibim la Eg-5 el fus serà monopolar ja que els centrosomes no se separaran. Els cromosomes es congregaran tot junts a sobre dels microtúbuls creats al voltant dels centrosomes units i la mitosi no podrà avançar correctament. La inhibició d’Eg-5 és un tractament efectiu per línees cel·lulars amb resistència al Taxol. Encara que de moment s’està provant en assaigs clínics, en el meu treball de laboratori utilitzaré la substància STLC per inhibir la proteïna Eg5 i observar què passa.
També s’estudia la inhibició de les proteïnes Aurora A i Polo-like cinasa-1 (Plk1), que estan sobre expressades en càncer i tenen papers importants en la fase G2 i la mitosi. Si les inhibim aconseguirem cèl·lules amb fusos d’un sol pol a causa del seu paper en la maduració i separació dels centrosomes en G2. Per tant la seva inhibició també pertorbaria la mitosi.
En els últims anys s’ha comprovat que un arrest mitòtic condueix a una mort cel·lular. S’han tractat cèl·lules amb fàrmacs antimitòtics que retarden la progressió de la mitosi durant un període extens de temps, i la majoria de vegades aquest retard és seguit per la mort cel·lular. Tot i així hi ha algun subconjunt de cèl·lules que poden escapar de la mort cel·lular i sortir d’aquest retard.
Sorprenentment hi ha una gran variació entre el moment de mort cel·lular entre cèl·lules dins d’una població genèticament idèntica. Ja que o bé moren en el punt de control mitòtic o poden sortir de la fase de mitosi i entrar un altre cop al cicle cel·lular. Però quan això passa tenen el material genètic duplicat cosa que portarà a la mort cel·lular posteriorment.
En els processos de les fases de la mitosi es consumeix molta energia, ja que estan actius processos com la condensació dels cromosomes, la formació del fus acromàtic, la congregació i segregació dels cromosomes. Tenint en compte que s’anul·len altres processos cel·lulars com per exemple el transport per vesícules. Per tant una mitosi prolongada pot resultar una privació d’energia important, cosa que no li interessa a la cèl·lula. Això fa que la cèl·lula sigui molt vulnerable durant la mitosi. També és vulnerable pel fet que el material genètic no està protegit per la membrana nuclear, cosa que fa que augmenti la sensibilitat de la cèl·lula respecte tractaments amb radiació .
Amb tot això les cèl·lules podrien haver dissenyat un procediment intrínsec (propi), com una via pre-apoptòtica, responsable de la separació de cèl·lules que passen massa temps en mitosi.
Segons dades recents s’ha observat que un retard mitòtic de tan sols 2 hores ja pot donar lloc a l’activació de p53 (una proteïna supressora tumoral), cosa que indica que una durada massa extensa d’aturada ja fa activar una resposta d’estrès en cèl·lules mitòtiques.
Concloent, una mitosi prolongada por resultar en l’activació de processos pre-apoptòtics, cosa que ens explica que les cèl·lules tenen certa sensibilitat a retardar-se en mitosis.
Una manera d’aconseguir la mort de les cèl·lules tumorals durant la mitosis és inhibir la degradació de la proteïna ciclina B. Si això passés les cèl·lules serien incapaces de sortir de la mitosi i es produiria una apoptosi abans que trobés la manera de sortir. En la part pràctica tractaré cèl·lules amb MG132, una substància que bloqueja el proteasoma i no deixa que es degradi la ciclina B.
Segons l’estudi de Huang i els seus alumnes al 2009, s’aconsegueix una major mort cel·lular inhibint la degradació de la ciclina B que fent servir fàrmacs que afectin el fus mitòtic.
Una altra manera específica d’interrompre la mitosi és fixant com a objectiu la citocinesis, un procés necessari per a les cèl·lules mitòtiques per ser físicament separades en dos cèl·lules filles.
La inhibició de la citocinesis donaria lloc a la formació d’una cèl·lula filla tetraploide, o sigui amb el doble del material genètic necessari.
Segons diferents estudis (Ditchfield 2003, Hauf 2003, Harrington 2004 i Kaestner 2009) la inhibició de la citocinesis resulta eficient per aconseguir la mort cel·lular en diferents línees tumorals. El millor és que no sembla tenir un efecte important sobre cèl·lules que no s’estan dividint, cosa que fa aquest objectiu encara més interessant contra la proliferació de cèl·lules cancerígenes.
Però com tots els mètodes, aquest també té els seus avantatges i desavantatges ja que un cop la tetraploïdia ja s’ha format poden passar diverses coses; la cèl·lula pot aturar el seu cicle cel·lular, i per tant acabar morint, durant la fase G1, o pot reduplicar el seu genoma i dividir-se un altre cop.
En els estudis de Janssen i Medema, van portar a terme la inhibició d’Aurora B, una cinasa important durant la mitosi, i van observar que aquesta inhibició era molt efectiva per aturar la mitosi perquè quan la cèl·lula sofria una tetraploïdia i continuava amb el seu cicle cel·lular de forma habitual, comptava amb un parell més de centrosomes. Això faria que la formació del fus mitòtic no fos correcta, es formaria més d’un fus (tipus d’error anomenat fus multipolar). La construcció d’aquest fus multipolar ocasiona que els cromosomes no es disposin correctament i, en el cas que la cèl·lula acabi dividint-se, que no es reparteixi la mateixa quantitat de material genètic en les dues cèl·lules filles (descendència aneuploide), cosa que assegura una viabilitat molt limitada, això vol dir que les cèl·lules moriran al cap de poc.
Tal com ja he formulat anteriorment, el problema es presenta quan una cèl·lula amb aquesta aneuploïdia és capaç de continuar el seu cicle cel·lular. Això el que fa és contribuir a la formació de cèl·lules cancerígenes i al creixement del tumor.
No obstant això, tal com mostren Shi i King en els seus estudis del 2005, la formació de fusos multipolars sovint acaben amb una mort cel·lular i no amb una descendència aneuploide.
S’observa que en un alt percentatge de cèl·lules tumorals humanes, en dividir-se, no es reparteix la mateixa quantitat de material genètic, hi ha cromosomes que perden o que guanyen parts. El fenotip resultant s’anomena CIN (de l’anglès chromosomal instability).
Les causes d’un fenotip CIN, són diverses i no gaire exactes. Se sap que si el fus no es construeix correctament, quan la cèl·lula es divideixi no anirà a parar la mateixa quantitat de material genètic a cada cèl·lula perquè els cromosomes no s’hauran disposat correctament. Però també hi ha altres estudis que revelen que aquesta inestabilitat cromosòmica és deguda a mutacions en gens necessaris per garantir una mitosi que progressi adequadament. Tot i haver trobat nombroses mutacions en aquests gens, no s’ha trobat cap mutació concreta que aparegui en un alt percentatge de tumors humans. Per tant, això suggereix que es poc probable que la inestabilitat cromosòmica sigui únicament causada per la inactivació o la mutació, dels gens que controlen la segregació cromosòmica, que s’encarreguen de suprimir els genomes que compten amb inestabilitat cromosòmica. Sinó que és més probable que sigui deguda a l’alteració de proteïnes que estan implicades en la protecció del genoma durant la divisió cel·lular.
Torres, al 2007, i Williams, al 2008, van observar que quan una cèl·lula tenia un cromosoma de més es disparava l’activació de vies d’estrès. Això passa perquè els gens dels cromosomes extres també són transcrits i la cèl·lula fa més feina del compte, de la que pot assumir, sintetitza massa proteïnes i consumeix massa energia.
Amb l’activació d’aquestes vies d’estrès, la cèl·lula amb aneuploïdia anirà creixent més lentament, perquè no té prou energia per fer-ho, i acabarà morint.
També són importants els punts de control que tenen lloc per controlar i assegurar que tot va seguint de la forma en que s’espera i que es pot continuar.
Aquestes vies de control són transitòries, o sigui desapareixen una vegada està resolt el problema que les ha posat en marxa i caduquen si el problema no s’ha resolt al cap d’un temps.
Lodish i els seus alumnes al 2005 van descriure els diferents punts de control que té el cicle cel·lular, per exemple n’hi ha un que s’anomena punt de control del dany del DNA, que pot funcionar en G1, S o G2, i ho fa de la següent manera: el dany genètic activarà la proteïna p53, que afavoreix la reparació del DNA i detindrà el cicle. En el cas que tot falli o que el dany sigui massa gran, estimularà l’apoptosi, la mort cel·lular programada.
- Cicle cel·lular i càncer
El càncer és una malaltia en que un grup de cèl·lules desenvolupen un creixement descontrolat, tenen una proliferació massa ràpida, es divideixen més enllà dels límits normals. Aquest grup de cèl·lules s’anomenen tumor i pot arribar a envair i destruir els teixits adjacents, i fins i tot pot escampar-se per diferents llocs del cos per via sanguínia o limfàtica i produir metàstasi.
Càncer i cicle cel·lular van molt lligats, perquè sabem que les cèl·lules cancerígenes es divideixen sense control, tenen un cicle cel·lular accelerat. Per tant una bona manera d’aturar el creixement d’un tumor, la proliferació de cèl·lules cancerígenes és deixar estancada la cèl·lula cancerígena en un dels estadis del cicle cel·lular, condemnant-la així a la impossibilitat de créixer més, de dividir-se i finalment a l’apoptosi.
La majoria de fàrmacs contra el càncer són fàrmacs que actuen contra la proliferació. Aquests fàrmacs el que fan és destorbar el cicle cel·lular, en diferents fases d’aquest. Per exemple n’hi ha que danyen el DNA o d’altres que funcionen com a inhibidors de cinasa dependent de ciclina.
Per tant hi ha diferents estratègies. En el meu treball he fixat la mitosi com si fos el “taló d’ Aquiles del càncer”, ja que sinó es pot realitzar la mitosi no es continua amb el cicle cel·lular i encara menys amb la proliferació cel·lular.
Medema i Jansen publicaren al 2011 un article explicant diversos procediments i investigacions portades a terme per poder frenar la proliferació de cèl·lules cancerígenes fixant la mitosis com a objectiu.
Una manera d’aturar la mitosi és allargar el punt de control de mitosi o de formació del fus acromàtic, ja que incrementar la durada de la mitosi acaba fent morir les cèl·lules mitòtiques. Hi ha substàncies com les taxanes i vinca alkaloids, una classe de drogues antimitòtiques que afecten la dinàmica dels microtúbuls. Causen formes anormals del fus acromàtic i això fa que els cromosomes no es puguin alinear correctament.
Quan això passa el punt de control s’atura, deixant un temps a la cèl·lula per corregir els errors, per tant s’està esperant massa estona per passar a l’anafase. Aquest temps d’espera ve donat per la senyal d’un grup de proteïnes.
Les substàncies que provoquen un alineament erroni dels cromosomes faran que la cèl·lula s’aturi en el punt de control de la mitosis, l’arrest mitòtic serà tan llarg que portarà la cèl·lula a la mort cel·lular. A part de portar a la mort cel·lular també s’ha vist en casos que es produeix una sortida de la mitosi (mitotic slippage), o sigui que la cèl·lula, tot i els seus errors, retrocedirà de fase mitòtica i tornarà a entrar en el cicle cel·lular. Però causarà una aneuploïdia perquè tornarà a començar el cicle cel·lular amb el doble de material genètic.
Les drogues convencionals microtubulars anomenades recentment (taxanes i vinca alkaloids) són efectives en alguns tractaments de càncer. Però hi ha una família de fàrmacs bastant nova, les Epothilones que són més suaus que les taxanes i tenen una estructura química que li fa tenir més afinitat pels microtúbuls. S’estan provant en assaigs clínics.
Però les substàncies que alteren la naturalesa dels microtúbuls tenen efectes secundaris. Aquests efectes es deuen a que aquestes substàncies impossibiliten la realització total i normal d’una mitosi (ja que els microtúbuls participen activament, formant el fus acromàtic), per tant frena la proliferació cel·lular a nivell general, no només el de cèl·lules cancerígenes. Aquesta frenada de la proliferació pot portar a una mielosupressió, una disminució de la medul·la òssia, disminuint així la producció d’eritròcits i de plaquetes. També és molt possible l’adquisició de certa resistència a aquests fàrmacs en diferents pacients segons com s’ha observat.
Per tant encara que veiem que l’acció de retardar la mitosi (efectiu amb aquests fàrmacs microtubulars) sembla tenir un efecte relativament citotòxic sobre el teixit cancerós, els efectes secundaris lligats a aquestes substàncies antimitòtiques en restringeixen l’aplicació.
Això va fer començar una recerca per trobar fàrmacs més selectius en quant a cèl·lules mitòtiques a les quals dirigir-se. Cal trobar punts febles de la mitosi per dissenyar fàrmacs específics.
Un dels objectius per aquest enfocament de tractament selectiu és fixar-se en la proteïna cinesina-5 (Eg5), una proteïna motora que pot unir-se a la superfície d’un microtúbul i desplaçar-s’hi longitudinalment arrossegant una càrrega mitjançant ATP com a font d’energia. La funció principal de la Eg5 és el transport de components cel·lulars. Doncs bé, aquesta proteïna durant la mitosi té la capacitat de portar a terme la separació dels centrosomes durant la profase, això iniciaria la construcció d’un fus acromàtic bipolar. Si inhibim la Eg-5 el fus serà monopolar ja que els centrosomes no se separaran. Els cromosomes es congregaran tot junts a sobre dels microtúbuls creats al voltant dels centrosomes units i la mitosi no podrà avançar correctament. La inhibició d’Eg-5 és un tractament efectiu per línees cel·lulars amb resistència al Taxol. Encara que de moment s’està provant en assaigs clínics, en el meu treball de laboratori utilitzaré la substància STLC per inhibir la proteïna Eg5 i observar què passa.
També s’estudia la inhibició de les proteïnes Aurora A i Polo-like cinasa-1 (Plk1), que estan sobre expressades en càncer i tenen papers importants en la fase G2 i la mitosi. Si les inhibim aconseguirem cèl·lules amb fusos d’un sol pol a causa del seu paper en la maduració i separació dels centrosomes en G2. Per tant la seva inhibició també pertorbaria la mitosi.
En els últims anys s’ha comprovat que un arrest mitòtic condueix a una mort cel·lular. S’han tractat cèl·lules amb fàrmacs antimitòtics que retarden la progressió de la mitosi durant un període extens de temps, i la majoria de vegades aquest retard és seguit per la mort cel·lular. Tot i així hi ha algun subconjunt de cèl·lules que poden escapar de la mort cel·lular i sortir d’aquest retard.
Sorprenentment hi ha una gran variació entre el moment de mort cel·lular entre cèl·lules dins d’una població genèticament idèntica. Ja que o bé moren en el punt de control mitòtic o poden sortir de la fase de mitosi i entrar un altre cop al cicle cel·lular. Però quan això passa tenen el material genètic duplicat cosa que portarà a la mort cel·lular posteriorment.
En els processos de les fases de la mitosi es consumeix molta energia, ja que estan actius processos com la condensació dels cromosomes, la formació del fus acromàtic, la congregació i segregació dels cromosomes. Tenint en compte que s’anul·len altres processos cel·lulars com per exemple el transport per vesícules. Per tant una mitosi prolongada pot resultar una privació d’energia important, cosa que no li interessa a la cèl·lula. Això fa que la cèl·lula sigui molt vulnerable durant la mitosi. També és vulnerable pel fet que el material genètic no està protegit per la membrana nuclear, cosa que fa que augmenti la sensibilitat de la cèl·lula respecte tractaments amb radiació .
Amb tot això les cèl·lules podrien haver dissenyat un procediment intrínsec (propi), com una via pre-apoptòtica, responsable de la separació de cèl·lules que passen massa temps en mitosi.
Segons dades recents s’ha observat que un retard mitòtic de tan sols 2 hores ja pot donar lloc a l’activació de p53 (una proteïna supressora tumoral), cosa que indica que una durada massa extensa d’aturada ja fa activar una resposta d’estrès en cèl·lules mitòtiques.
Concloent, una mitosi prolongada por resultar en l’activació de processos pre-apoptòtics, cosa que ens explica que les cèl·lules tenen certa sensibilitat a retardar-se en mitosis.
Una manera d’aconseguir la mort de les cèl·lules tumorals durant la mitosis és inhibir la degradació de la proteïna ciclina B. Si això passés les cèl·lules serien incapaces de sortir de la mitosi i es produiria una apoptosi abans que trobés la manera de sortir. En la part pràctica tractaré cèl·lules amb MG132, una substància que bloqueja el proteasoma i no deixa que es degradi la ciclina B.
Segons l’estudi de Huang i els seus alumnes al 2009, s’aconsegueix una major mort cel·lular inhibint la degradació de la ciclina B que fent servir fàrmacs que afectin el fus mitòtic.
Una altra manera específica d’interrompre la mitosi és fixant com a objectiu la citocinesis, un procés necessari per a les cèl·lules mitòtiques per ser físicament separades en dos cèl·lules filles.
La inhibició de la citocinesis donaria lloc a la formació d’una cèl·lula filla tetraploide, o sigui amb el doble del material genètic necessari.
Segons diferents estudis (Ditchfield 2003, Hauf 2003, Harrington 2004 i Kaestner 2009) la inhibició de la citocinesis resulta eficient per aconseguir la mort cel·lular en diferents línees tumorals. El millor és que no sembla tenir un efecte important sobre cèl·lules que no s’estan dividint, cosa que fa aquest objectiu encara més interessant contra la proliferació de cèl·lules cancerígenes.
Però com tots els mètodes, aquest també té els seus avantatges i desavantatges ja que un cop la tetraploïdia ja s’ha format poden passar diverses coses; la cèl·lula pot aturar el seu cicle cel·lular, i per tant acabar morint, durant la fase G1, o pot reduplicar el seu genoma i dividir-se un altre cop.
En els estudis de Janssen i Medema, van portar a terme la inhibició d’Aurora B, una cinasa important durant la mitosi, i van observar que aquesta inhibició era molt efectiva per aturar la mitosi perquè quan la cèl·lula sofria una tetraploïdia i continuava amb el seu cicle cel·lular de forma habitual, comptava amb un parell més de centrosomes. Això faria que la formació del fus mitòtic no fos correcta, es formaria més d’un fus (tipus d’error anomenat fus multipolar). La construcció d’aquest fus multipolar ocasiona que els cromosomes no es disposin correctament i, en el cas que la cèl·lula acabi dividint-se, que no es reparteixi la mateixa quantitat de material genètic en les dues cèl·lules filles (descendència aneuploide), cosa que assegura una viabilitat molt limitada, això vol dir que les cèl·lules moriran al cap de poc.
Tal com ja he formulat anteriorment, el problema es presenta quan una cèl·lula amb aquesta aneuploïdia és capaç de continuar el seu cicle cel·lular. Això el que fa és contribuir a la formació de cèl·lules cancerígenes i al creixement del tumor.
No obstant això, tal com mostren Shi i King en els seus estudis del 2005, la formació de fusos multipolars sovint acaben amb una mort cel·lular i no amb una descendència aneuploide.
S’observa que en un alt percentatge de cèl·lules tumorals humanes, en dividir-se, no es reparteix la mateixa quantitat de material genètic, hi ha cromosomes que perden o que guanyen parts. El fenotip resultant s’anomena CIN (de l’anglès chromosomal instability).
Les causes d’un fenotip CIN, són diverses i no gaire exactes. Se sap que si el fus no es construeix correctament, quan la cèl·lula es divideixi no anirà a parar la mateixa quantitat de material genètic a cada cèl·lula perquè els cromosomes no s’hauran disposat correctament. Però també hi ha altres estudis que revelen que aquesta inestabilitat cromosòmica és deguda a mutacions en gens necessaris per garantir una mitosi que progressi adequadament. Tot i haver trobat nombroses mutacions en aquests gens, no s’ha trobat cap mutació concreta que aparegui en un alt percentatge de tumors humans. Per tant, això suggereix que es poc probable que la inestabilitat cromosòmica sigui únicament causada per la inactivació o la mutació, dels gens que controlen la segregació cromosòmica, que s’encarreguen de suprimir els genomes que compten amb inestabilitat cromosòmica. Sinó que és més probable que sigui deguda a l’alteració de proteïnes que estan implicades en la protecció del genoma durant la divisió cel·lular.
Torres, al 2007, i Williams, al 2008, van observar que quan una cèl·lula tenia un cromosoma de més es disparava l’activació de vies d’estrès. Això passa perquè els gens dels cromosomes extres també són transcrits i la cèl·lula fa més feina del compte, de la que pot assumir, sintetitza massa proteïnes i consumeix massa energia.
Amb l’activació d’aquestes vies d’estrès, la cèl·lula amb aneuploïdia anirà creixent més lentament, perquè no té prou energia per fer-ho, i acabarà morint.